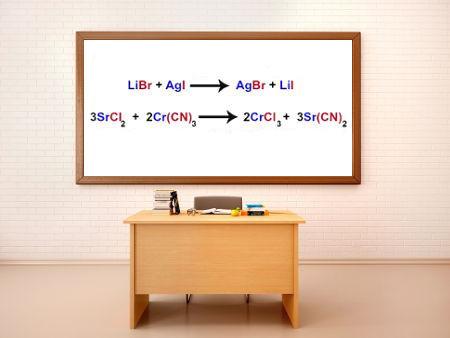
Esse tipo de reação também é denominada de reação de metátese, porque essa palavra é de origem grega (methatesis), que significa “transposição”. É exatamente isso o que ocorre com os átomos, grupos de átomos ou os íons dos compostos reagentes; eles são trocados.
Genericamente, temos:
AB + XY → AY + XB
Para que uma reação de dupla troca ou de metátese ocorra, ela deve estar em uma das três situações abaixo:
(1ª) Pelo menos um dos produtos deve ser mais fraco (menos ionizado ou dissociado) que os reagentes.
Exemplo: Uma reação de neutralização ou salificação (ácido + base originado sal + água) entre o ácido clorídrico e o hidróxido de sódio:
HCl + NaOH →NaCl + H2O
Nesse caso, o ácido clorídrico é um ácido muito ionizado e o hidróxido de sódio é uma base muito dissociada, já a água (produto) é uma substância pouco ionizada.
(2ª) Pelo menos um dos produtos deve ser mais volátil que os reagentes:
Uma substância volátil é aquela que passa com facilidade do estado líquido para o gasoso (vaporização) em condições ambientes.
Exemplo: Reação entre o bicarbonato de sódio e o ácido clorídrico. Observe que o ácido carbônico que é formado é tão volátil que se decompõe originando gás carbônico.
NaHCO3 + HCl →NaCl + H2CO3 → NaCl +CO2 +H2O
(3ª) Pelo menos um dos produtos é menos solúvel que os reagentes:
Isso significa que ocorrerá a formação de um precipitado nessa situação.
Exemplo: Quando se adiciona cal hidratada a uma solução aquosa de sulfato de alumínio (substância coagulante usada para floculação no tratamento de água), o cálcio se une ao sulfato, e o alumínio se liga ao hidróxido, dando origem a um precipitado branco.
3 Ca(OH)2(aq) + Al2(SO4)3(aq) → 2 Al(OH)3(aq) + 3 CaSO4(s)
Outro exemplo, que pode ser visto na figura abaixo, é a precipitação do iodeto de chumbo (amarelo) quando misturamos duas soluções aquosas de nitrato de chumbo e iodeto de sódio:
Pb(NO3)2(aq) + NaI(aq) → PbI2(s) + 2 NaNO3(aq)
Reação de dupla troca com formação de precipitado de iodeto de chumbo Título: Precipitado iodeto de chumbo