O termo raio atômico (RA), uma propriedade periódica dos elementos químicos, refere-se ao tamanho de um átomo. Mas vale salientar que a determinação experimental dessa propriedade não pode ser realizada com precisão.
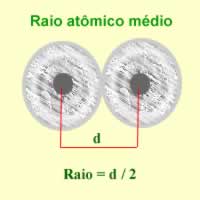
Para se ter uma noção do raio de um átomo, utiliza-se um feixe de raio X que atravessa uma amostra do elemento químico que se deseja determinar o raio. Como o material apresenta vários átomos na sua constituição, eles promovem um desvio do feixe de raio X, que, por sua vez, deixa uma imagem dos núcleos atômicos em um filme fotográfico. Ao estudar a imagem formada no filme fotográfico, verifica-se a posição do núcleo dos átomos. Assim, a medida do raio atômico é feita pela divisão da distância entre os núcleos de dois átomos por 2.
.jpg)
Representação da imagem de dois núcleos de átomos em um filme fotográfico
Assim:
RA = d/2
É importante ressaltar que no estudo do raio atômico a força de atração entre os prótons do núcleo e os elétrons dos níveis é determinante para avaliar o raio de um átomo, ou seja, quanto mais os prótons do núcleo atraem os elétrons para perto de si, menor é o tamanho do átomo.
A partir da definição de raio atômico, é possível compreender o raio iônico. Define-se como raio iônico o tamanho de um íon. Essa propriedade é estudada quando um átomo perde ou ganha elétrons (íons).
Obs.: Quando o íon é um átomo que perdeu elétrons, nós o chamamos de cátion; mas quando ele é um átomo que ganhou elétrons, ele é chamado de ânion. A seguir temos as representações genéricas de um cátion e de um ânion:
X+ (cátion) Y-(ânion)
Quando o átomo apresentar o seu número de elétrons aumentado (ânion) ou diminuído (cátion), a força de atração do núcleo será influenciada, modificando consequentemente o raio do átomo.
A influência da perda ou ganho de elétrons será avaliada de forma individual e de acordo com os itens a seguir:
a) Raio de um cátion
Quando um átomo neutro (número de prótons igual ao número de elétrons) perde um elétron, ele transforma-se em um cátion. Como o núcleo agora tem um número de prótons maior em relação ao número de elétrons, ele acaba atraindo mais para perto de si os elétrons dos níveis, o que gera uma redução do tamanho do átomo. Abaixo temos um exemplo da formação do cátion de um átomo de lítio a partir de um átomo de lítio neutro.

Formação do cátion do lítio pela perda de um elétron do segundo nível
b) Raio de um ânion
Quando um átomo neutro (número de prótons igual ao número de elétrons) ganha um elétron, ele transforma-se em um ânion. Como o núcleo agora tem um número de prótons menor em relação ao número de elétrons, a atração que o núcleo exerce sobre os elétrons é superada pelas forças de repulsão entre os elétrons nos níveis. Assim, o átomo terá o seu raio ampliado em razão do afastamento entre os elétrons. A seguir temos um exemplo da formação do ânion de um átomo de boro a partir de um átomo de boro neutro.

Formação do ânion do boro pelo ganho de três elétrons no segundo nível