O creme dental é um produto indispensável para a manutenção da saúde dos dentes, pois, além de combater as cáries, ele ajuda também no combate ao tártaro, à placa bacteriana e auxilia até no clareamento dos dentes.
Mas quais são as substâncias presentes nos cremes dentais que possibilitam todas essas funções?
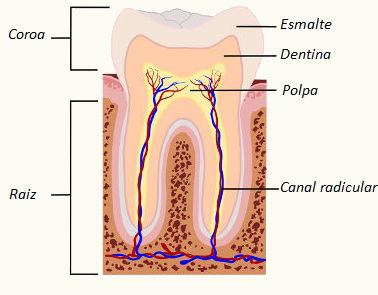
Primeiramente, vejamos alguns detalhes sobre a química dos dentes. O principal constituinte do esmalte dos dentes é a hidroxiapatita, que é um sal com a seguinte fórmula molecular: Ca5OH(PO4)3(s). Esse sal é duro e é praticamente insolúvel em água, no entanto ele pode ser atacado por ácidos.
A hidroxiapatita, que está em meio aquoso, por causa da saliva, entra em equilíbrio com os seus íons, conforme a equação química abaixo. A dissolução da hidroxiapatita é denominada desmineralização; e o processo inverso, mineralização.

A presença de ácidos em nossa boca fará com que haja íons H+, que irão reagir com as hidroxilas (OH-), provocando um deslocamento do equilíbrio da reação acima no sentido da reação direta. Isso significa que a desmineralização será favorecida, a hidroxiapatita vai ser mais consumida e irá fragilizar o esmalte dos dentes.
A presença de ácidos pode se dar principalmente de duas formas: a primeira é por meio do consumo de comidas e bebidas ácidas, como refrigerantes. Já outra forma de o meio ficar ácido acontece da seguinte maneira: a nossa saliva possui proteínas que formam uma camada invisível sobre os dentes. Nessa camada, acumulam-se as bactérias e a esse conjunto é que damos o nome de placa bacteriana ou biofilme. Quando comemos açúcares e proteínas, as bactérias também se alimentam deles e os metabolizam, liberando ácidos que atacam os dentes, dissolvendo o esmalte e provocando a cárie.
Para combater esse processo de desmineralização da hidroxiapatita, os cremes dentais costumam dizer em suas embalagens que contêm flúor (F). Mas, na realidade, esse termo é incorreto; pois todos os cremes dentais contêm o íon fluoreto (F1-) que vem em sais, como o monoflúor fosfato de sódio (Na4(PO4)F) e o fluoreto de sódio (NaF).
A presença do fluoreto é importante porque ele tem a propriedade de substituir os íons hidroxila (OH-) na hidroxiapatita, formando o composto fluorapatita, que é ainda menos solúvel em água e torna o esmalte dos dentes mais resistente ao ataque dos ácidos, pois não se forma a hidroxila em sua dissociação:

Visto que o meio ácido favorece a formação de cáries, alguns cremes dentais contêm também certas bases que diminuem a acidez da boca, como o bicarbonato de sódio e o hidróxido de magnésio.
Assim, o uso de do fio dental e do creme dental em uma escovação correta retira a placa bacteriana que se forma e previne o tártaro, que é uma deposição de sais minerais sobre os dentes, que ocorre quando a placa não é removida. O tártaro é uma estrutura rígida que não é retirada só com a escovação, sendo necessário ir ao dentista.
A ação anticárie que é destacada pelo marketing se dá em virtude da presença do íon fluoreto. Já a ação antitártaro é conseguida com a presença de peróxidos ou pirofosfatos. E, como vimos, a placa contém bactérias, por isso os cremes dentais com ação antiplaca bacteriana contêm substâncias antimicrobianas. A ação clareadora se dá em razão da presença de água oxigenada.
Outro aspecto interessante do creme dental é a espuma que ele faz, sendo, portanto, considerado um detergente, assim como outros produtos que geram espuma, como xampus, detergentes sintéticos, sabões e sabonetes. Essa espuma é resultado da presença do laurilssulfato de sódio em sua composição. Sua fórmula está esquematizada abaixo:
H3C ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ CH2 ─ OSO-3Na+