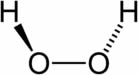Os compostos que pertencem à função inorgânica dos óxidos são caracterizados por serem binários, isto é, formados por apenas dois elementos diferentes, sendo que o mais eletronegativo deles é o oxigênio.
Existem vários óxidos importantes e com inúmeras aplicações em nosso cotidiano. A seguir trataremos dos principais:
1- Principais óxidos básicos (óxidos que reagem com água, originando uma base; e reagem com ácido, originando sal e água como produtos):
- CaO (Óxido de cálcio):
A obtenção desse composto é feita através do aquecimento do CaCO3, conforme a reação abaixo, sendo que o CaCO3 é encontrado no mármore, calcário e na calcita:
![]()
O óxido de cálcio é normalmente conhecido por cal virgem ou cal viva, sendo que misturado à água dá origem à cal extinta ou cal apagada, ou ainda cal hidratada (Ca(OH)2). É utilizado principalmente em construções, no preparo de argamassa, cimento e cerâmicas; e na agricultura, para diminuir a acidez (pH) do solo.

- Óxido de magnésio (MgO):
Esse composto, ao ser misturado com água, dá origem ao conhecido leite de magnésia, que é o hidróxido de magnésio usado como antiácido estomacal.

2- Principais óxidos ácidos (óxidos que reagem com água, originando um ácido; e reagem com uma base, originando sal e água como produtos):
- Dióxido de Carbono (CO2):
O dióxido de carbono ou gás carbônico é um composto que está presente principalmente na atmosfera, pois é proveniente da respiração de plantas e animais, além da queima de combustíveis. Ele faz parte do processo de fotossíntese realizado pelas plantas.
O gás carbônico é muito utilizado como gás de refrigerantes e de água gaseificada, que ocasiona um meio ácido ao reagir com a água.
Quando está no estado sólido, ele é denominado gelo-seco, pois passa diretamente do estado sólido para o gasoso, à temperatura ambiente. Ele é muito usado para gerar o efeito de fumaça em shows, teatro, filmes e outros eventos e espetáculos.
- Óxido de silício (SiO2):
Esse composto é conhecido normalmente como sílica e representa o óxido mais abundante na crosta terrestre. Sua principal fonte de obtenção é a areia, mas pode também ser encontrado em diversas formas cristalinas, como quartzo puro (foto), topázio e ametista. Sua principal aplicação é na produção de vidro.

3- Principal peróxido (óxidos que apresentam em sua estrutura o grupo (O2)2-):
- Peróxido de hidrogênio (H2O2):
O peróxido de hidrogênio, quando está em meio aquoso (H2O2(aq)), origina a chamada água oxigenada, sendo que suas soluções aquosas diluídas são muito utilizadas para clarear os pelos do corpo e os fios de cabelo. Além disso, quando apresenta a concentração de apenas 3%, ela é usada como agente bactericida, antisséptico e alvejante. Com a concentração acima de 30%, seu uso é feito somente em indústrias, como em alvejante de madeiras, fibras têxteis e na propulsão de foguetes.
Esse composto explode violentamente quando aquecido e entra em decomposição ao ser exposto à luz.

4- Principal óxido neutro (óxidos que não reagem com água, ácido ou base):
- Monóxido de carbono (CO):
Gás extremamente tóxico que pode causar sintomas variados, como dor de cabeça, problemas na visão e até a morte se a exposição a esse gás for muito grande. Algumas formas de exposição a ele são o fumo passivo e a poluição atmosférica.
Ele pode ser usado para produzir metanol, por se combinar com o gás hidrogênio, mas sua principal aplicação é nas siderúrgicas, onde reage com o óxido de ferro III da hematita para produzir ferro metálico.

Aproveite para conferir nossas videoaulas sobre o assunto: