A pilha também é denominada célula galvânica e fornece energia ao sistema somente até que a reação química se esgote.
Seu funcionamento se baseia em transferência de elétrons de um metal que tem a tendência de ceder elétrons para um que tem a tendência de ganhar elétrons, ou seja, ocorrem reações de oxidorredução. Essa transferência é feita por meio de um fio condutor.
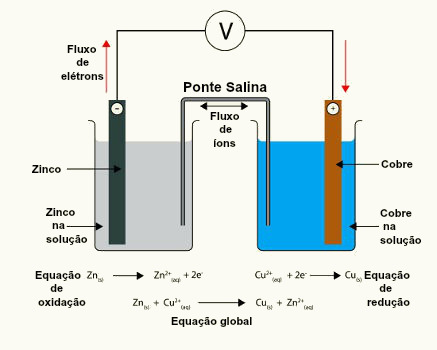
Para entendermos como isso se dá, vejamos a reação de oxidorredução que ocorre entre o zinco e o cobre e como isso pode ser utilizado para gerar uma pilha:
Se colocarmos uma placa de zinco em uma solução de sulfato de zinco (ZnSO4), estaremos constituindo um eletrodo de zinco. Da mesma maneira, se colocarmos uma placa de cobre em uma solução de sulfato de cobre (CuSO4), teremos um eletrodo de cobre.
Como o zinco é mais reativo que o cobre, ele tem a tendência de doar elétrons para o cobre. Assim, se ligarmos esses dois eletrodos por meio de um fio condutor externo, ocorrerá a transferência dos elétrons e consequentemente a passagem de corrente elétrica. Isso é visível, pois, depois de um tempo, notamos que a lâmina de cobre teve um aumento em sua massa, enquanto que a de zinco sofreu corrosão.
Os elétrons, por apresentarem carga negativa, migram do eletrodo negativo, denominado ânodo; para o positivo, que recebe o nome de cátodo. Assim, temos a reação global dessa pilha em particular:
Semirreação do ânodo: Zn (s) → Zn2+ (aq) + 2 e-
Semirreação do cátodo: Cu2+(aq) + 2e- →Cu(s)___________
Reação global da pilha: Zn (s) + Cu2+(aq)→ Zn2+ (aq) + Cu(s)

A notação química correta de uma pilha baseia-se na seguinte regra por convenção mundial:
Ânodo // Cátodo
Oxidação // redução
Assim, nesse casso, temos:
Zn / Zn2+ // Cu2+ //Cu(s)
Isso mostra que esse dispositivo é uma pilha, pois a partir de uma reação espontânea de oxidorredução ele produziu corrente elétrica. Essa pilha é chamada de Pilha de Daniell, por ter sido construída em 1836, pelo químico e meteorologista inglês John Frederic Daniell (1790-1845).
Hoje existe uma diversidade de pilhas que podem variar em diferentes aspectos. Porém, as pilhas mais comuns são as secas, que não utilizam soluções aquosas como as da Pilha de Daniell; mas que funcionam baseadas no mesmo princípio: a transferência de elétrons do ânodo para o cátodo. A seguir temos a representação esquemática da composição de uma pilha seca ácida:

Aproveite para conferir nossa videoaula sobre o assunto: