Ligação Covalente é a união estabelecida entre átomos por meio de pares de elétrons, ou seja, há um compartilhamento de elétrons.
Para entendermos melhor tal conceito, consideremos o caso do gás oxigênio (O2).
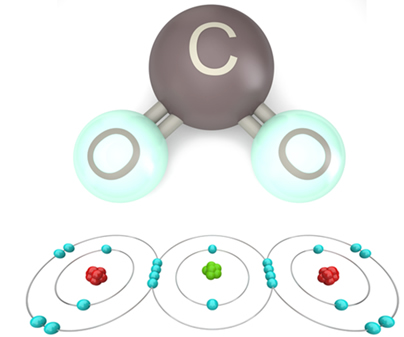
A estabilidade eletrônica é alcançada quando o átomo atinge a configuração eletrônica semelhante à de um gás nobre, isto é, com oito elétrons na última camada. Desse modo, o oxigênio, que possui seis elétrons na camada de valência, precisará ganhar dois elétrons para se tornar estável. Assim, conforme a figura abaixo, os átomos de oxigênio compartilham dois pares de elétrons para ambos ficarem estáveis.

Formação da molécula simples de oxigênio por meio da ligação covalente.
Desse modo, as estruturas formadas são eletricamente neutras. Os pares eletrônicos ligados não são doados nem recebidos de um átomo para o outro, eles são na verdade compartilhados, aparecendo simultaneamente em ambos os átomos. Portanto, são contados como constituintes de ambas as eletrosferas.
Os “pontinhos” ou os “xis”, ao redor dos átomos de oxigênio representam os seus elétrons da última camada. Essa forma de representação é chamada de Fórmula Eletrônica ou Fórmula de Lewis em homenagem ao químico Gilbert Newton Lewis (1875-1946), que a criou. Ele criou também a teoria das ligações covalentes imaginando os elétrons orientados em certas direções, nas quais formariam ligações químicas.
A última forma de representação mostrada no exemplo acima é chamada de Fórmula Estrutural Plana ouFórmula Estrutural de Couper, em que cada par de elétrons entre dois átomos pode ser representado por um traço. Nesse caso, temos dois traços ou uma ligação dupla. Abaixo, temos o esquema das possíveis ligações:

Esquema das três possíveis ligações covalentes
Essa ligação é feita somente entre átomos com tendências de ganhar elétrons, ou seja, somente entre ametais, semimetais e hidrogênio.
Outros casos de Ligação Covalente estão mostrados a seguir:
- Substâncias simples: formadas por átomos de um mesmo elemento.
H2

Ligação covalente do gás hidrogênio.
Cl2

Ligação covalente da molécula de cloro.
N2

Ligação covalente da molécula do nitrogênio.
- Substâncias compostas: formadas por dois ou mais elementos diferentes.
H2O

Ligação covalente da água.
CO2

Ligação covalente do gás carbônico.