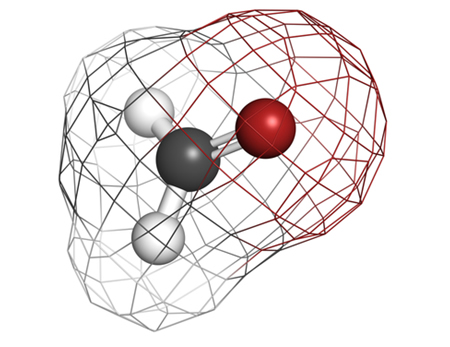
Na hibridização do Berílio, dois orbitais (um do tipo s e outro do tipo p) presentes na camada de valência de um átomo de berílio unem-se e originam dois orbitais híbridos do tipo sp.
Esse fenômeno é fundamental para que os átomos desse elemento químico sejam capazes de realizar duas ligações do tipo covalente sigma, principalmente se levarmos em consideração o fato de o berílio ser um elemento metálico, isto é, com tendência de realizar ligações iônicas, e não covalentes.
De forma simples, identificamos que um átomo de Berílio está realizando a hibridização sp e, consequentemente, duas ligações covalentes sigma sempre que tivermos uma molécula em que o berílio está interagindo com um ametal ou com átomos de hidrogênio.
![]()
Representação estrutural do Berílio cuja hibridização é do tipo sp
Berílio em seu estado fundamental
Em seu estado fundamental, o Berílio, cujo número atômico é 4, apresenta a seguinte distribuição eletrônica:
.jpg)
Ele possui uma camada de valência (sendo ela o segundo nível) com dois elétrons no subnível s. Esses dois elétrons estão posicionados no orbital com spins contrários, segundo a regra de Hund.
.jpg)
Formas de representação dos orbitais do berílio no estado fundamental
Berílio em seu estado excitado
Quando um átomo de Berílio recebe energia do meio externo, os elétrons da camada de valência absorvem essa energia e ficam excitados, ampliando ainda mais sua movimentação.
.jpg)
Chegada da energia em um átomo de berílio
Com isso, dificilmente dois elétrons continuam ocupando um mesmo orbital. Assim, um elétron que estava localizado no orbital do subnível s (do segundo nível) é deslocado para um dos orbitais do subnível p vazios (também do segundo nível).
.jpg)
Representação dos orbitais do Berílio no estado excitado
Berílio em seu estado hibridizado
Após a excitação do átomo de Berílio, os orbitais presentes na camada de valência sofrem a hibridização, ou seja, unem-se. Assim, temos a união de um orbital incompleto do subnível s com um orbital incompleto do subnível p, o que resulta em dois orbitais híbridos do tipo sp.
.jpg)
Representação dos orbitais do Berílio no estado hibridizado
Aproveite para conferir nossa videoaula sobre o assunto: