A estereoquímica é um ramo da Química Orgânica que estuda as diversas possibilidades de estruturas em três dimensões das moléculas de carbono e suas consequências, isto é, as propriedades químicas resultantes.
Uma parte importante da estereoquímica é a estereoisomeria, que ocorre quando dois ou mais compostos são isômeros (palavra que vem do grego isoméres = “partes iguais”) ou, mais corretamente nesse caso, estereoisômeros, que são compostos com a mesma fórmula molecular, mas que se diferenciam unicamente pelo arranjo tridimensional de seus substituintes.
Isso quer dizer que esses compostos pertencem ao mesmo grupo funcional, possuem a mesma estrutura esqueletal (quando se considera a fórmula estrutural plana), além de a insaturação, heteroátomo ou substituinte (se houver) e grupo funcional estarem no mesmo carbono da cadeia. A única diferença é realmente o arranjo dos átomos no espaço, o que resulta em propriedades totalmente diferentes. Por isso, a importância de estudar as características das figuras geométricas que apresentam duas ou três dimensões.
Existem fórmulas estereoquímicas que permitem relacionar as propriedades dos compostos com a disposição espacial dos seus átomos. Vejamos os três casos principais de estereoisomeria (isômeros conformacionais, enantiômeros e diastereoisômeros) e como podem ser representados por diferentes projeções:
1. Isômeros conformacionais: São aqueles estereoisômeros que podem interconverter-se um no outro somente por meio da rotação que ocorre em torno da ligação simples. Portanto, isso ocorre somente em compostos saturados, ou seja, que possuem apenas ligações simples entre carbonos.
Uma das formas de representar essas conformações é por meio das projeções de Newman, que mostram o que um observador veria se olhasse para a molécula no sentido de uma das ligações carbono-carbono. Essa ligação é representada por um circulo central e os ligantes dos dois carbonos da ligação considerada ficam ao redor.
Veja, por exemplo, a projeção de Newman para duas conformações do etano:
Fórmula estrutural plana do etano: H H
│ │
H ─ C ─ C ─ H
│ │
H H
Projeções de Newman:

Projeções de Newman para etano
A molécula do etano na conformação I-estrela, também chamada de “anti”, é a mais estável porque os seus substituintes estão afastados o máximo possível, passando por um mínimo de energia potencial. Conforme há a rotação, essa energia vai aumentando. Ao adquirir a conformação II- eclipse (ou syn), a energia atinge o seu máximo. Essa conformação é então a mesmos estável. Veja que os substituintes estão bem próximos uns dos outros. Dessa forma, a maioria das moléculas do etano encontra-se na forma anti, ou seja, na conformação mais estável.
Outra forma de representar essas diferentes conformações é a fórmula em cavalete. Veja como fica esse tipo de representação para o etano:

Fórmulas de cavalete para etano
Uma terceira representação é a fórmula de Fischer, em que cada carbono e as suas quatro ligações são representados por uma espécie de cruz, na qual o átomo central (carbono) encontra-se no ponto de intersecção. As linhas horizontais representam as ligações que estão na direção do observador (para a frente do plano do papel), e as linhas verticais, as ligações que se afastam do utilizador (para trás do plano do papel).
Veja um exemplo de fórmulas de Fischer para as moléculas de glicose e frutose:

Fórmulas de Fischer para glicose e frutose
A última forma de representar esses compostos para estudar sua conformação espacial é por meio da fórmula de perspectiva de Haworth. Nela, as fórmulas das substâncias não se encontram de forma exatamente plana no espaço e, por isso, para dar uma ideia mais espacial, as ligações podem indicar se o átomo está no plano (traço normal), atrás do plano (cunha pontilhada) ou à frente do plano (cunha cheia):

Representações em fórmulas em perspectiva
Veja um exemplo abaixo em que um esteroide é representado por uma fórmula de Haworth. Repare que dois hidrogênios estão atrás do plano, enquanto dois grupos metil, um hidrogênio e uma hidroxila estão à frente do plano, mais próximos do observador. A fórmula em 3D modelo bola-e-vara logo a seguir comprova isso:

Representação da estrutura de um esteroide por meio da fórmula de Haworth e de bola-e-vara
2 – Enantiômeros:
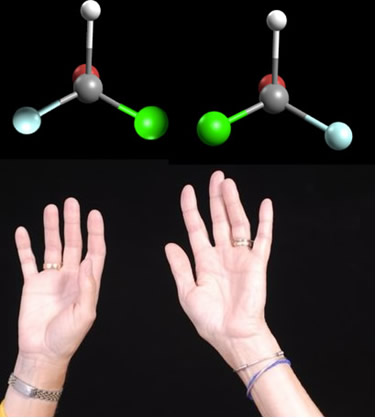
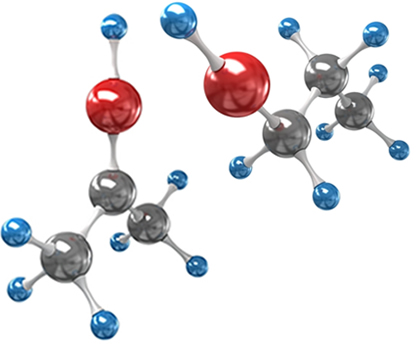
Os enantiômeros são compostos que são a imagem especular um do outro, mas não são sobreponíveis. Isso ocorre, por exemplo, com compostos quirais ou assimétricos que possuem pelo menos um carbono quiral, isto é, com os quatro ligantes diferentes.
Essa palavra “quiral” significa 'mão' em grego. Os enantiômeros atuam exatamente como ocorre com a nossa mão, ou seja, as nossas mãos são assimétricas (se você dividir a sua mão em duas partes elas serão diferentes), não se sobrepõem (coloque uma mão em cima da outra com as palmas voltadas para o seu rosto e verá que os dedos de uma mão não ficam em cima dos dedos respectivos da outra mão) e são a imagem especular uma da outra (se você colocar a mão direita na frente de um espelho, a imagem dela será exatamente igual à mão esquerda).
Os enantiômeros possuem a diferença física de desviar o plano de vibração da luz polarizada para sentidos opostos e isso resulta em diferentes propriedades químicas. Entenda mais sobre isso lendo os textos:
- ISOMERIA ÓPTICA ;
- A QUIRALIDADE E A INDÚSTRIA FARMACÊUTICA;
- CARBONO ASSIMÉTRICO OU QUIRAL.
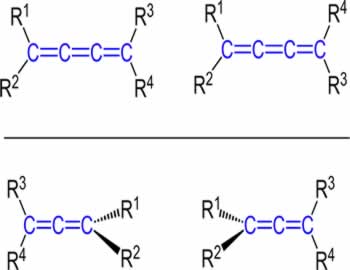
3- Diastereoisômeros:
Os diastereoisômeros são compostos que não são a imagem especular um do outro. Nesses casos, há pelo menos uma dupla ligação entre dois carbonos na cadeia aberta e ocorre a estereoisomeria do tipo geométrica ou cis-trans. Leia sobre ela nos textos abaixo: