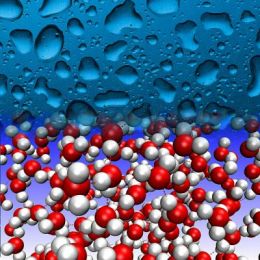
Água, gelo, vapor representam os três estados físicos que a matéria pode adquirir.
Vejamos cada um em particular:
Estado sólido: se caracteriza pela proximidade entre as moléculas, o que dá forma e volume fixos à matéria. As forças de coesão (atração) predominam no estado sólido.
Exemplo: O gelo possui forma e volume constantes, e ao menos que passe por aquecimento, dizemos que se encontra no estado sólido e que não sofre compressão. O gelo é resultante do congelamento de um líquido.
Estado líquido: as moléculas estão mais afastadas do que no estado sólido.
A matéria, quando se encontra nesse estado, possui forma variada, mas volume constante. A água líquida, por exemplo, possui facilidade de escoamento e adquire a forma do recipiente que a contém.
Estado gasoso: as forças de repulsão passam a existir causando um movimento das moléculas, estas querem se afastar umas das outras.
Neste estado a matéria pode ser comprimida se operarmos uma força externa, ela não tem forma e nem volume constante e sofre compressão e expansão facilmente. Portanto, se variarmos a pressão exercida sobre um gás, podemos aumentar ou diminuir o volume dele. Dizemos então que um gás tem a forma do recipiente que o contém, e se tiver livre no ar não adquire forma alguma.
O vapor d’água é um exemplo do estado gasoso da matéria, ele é produto do aquecimento de um líquido.
Agora podemos concluir que Água, gelo, vapor têm em comum a matéria constituinte (H2O), mas em diferentes estados físicos: líquido, sólido e gasoso.
Aproveite para conferir nossas videoaulas sobre o assunto: