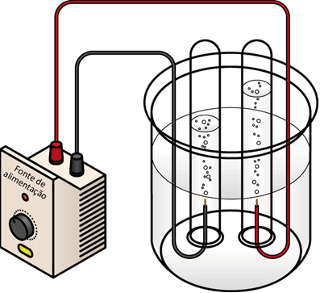
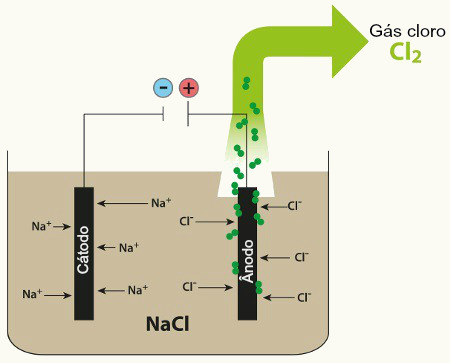
A eletrólise é um processo que transforma energia elétrica em energia química por meio da passagem de corrente elétrica numa substância no estado líquido, fundida, ou em meio aquoso. Nesse processo, os eletrodos usados podem ser inertes ou ativos.
Os eletrodos inertes mais usados são os de grafita e platina, e eles não participam da reação de oxirredução, apenas conduzem os elétrons.
Já no caso dos eletrodos não inertes ou ativos, eles sofrem oxidação e redução, participando da reação química.
O exemplo mais importante da utilização de eletrodos ativos é o da purificação eletrolítica do cobre. O cobre metalúrgico geralmente é obtido por meio do minério calcosita (Cu2S) não puro. Mas, para ser usado, principalmente em fios elétricos, ele precisa ter um alto grau de pureza (99,9%), o que pode ser conseguido através da eletrólise.
Isso é feito colocando-se no cátodo (eletrodo negativo da eletrólise) uma placa de cobre puro e no ânodo (eletrodo positivo) uma placa de cobre impuro, que é a que queremos purificar. Ambos ficam mergulhados numa solução de sulfato de cobre (CuSO4).
Ocorre, então, a oxidação do ânodo, em que cada átomo de cobre perde dois elétrons e os íons Cu2+ são liberados para o meio. Já no cátodo ocorre a sua redução, pois tanto os íons Cu2+ liberados pelo ânodo quanto os íons Cu2+ presentesna solução são atraídos por ele (pois o cátodo é negativo e cargas opostas se atraem) e se depositam nesse eletrodo.

As semirreações em cada eletrodo são as seguintes:
Semirreação do ânodo: Cu0(s)→ Cu2+(aq) + 2e-
Semirreação do cátodo: Cu2+(aq) + 2e- → Cu0(s)
Reação Global: zero
O resultado da reação global é igual a zero porque na verdade não ocorreu uma transformação química, apenas um transporte do cobre do ânodo para o cátodo. Dessa forma, no eletrodo negativo (cátodo), obtém-se o cobre purificado.