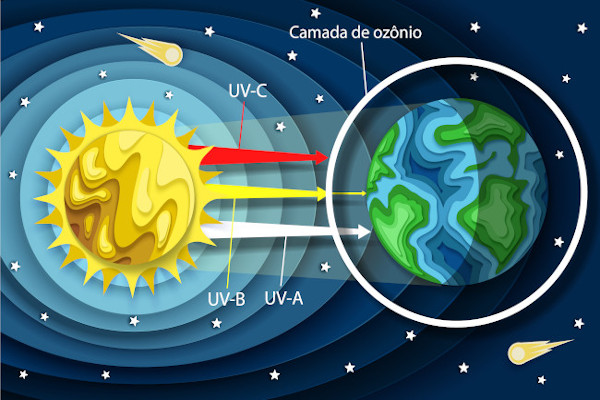
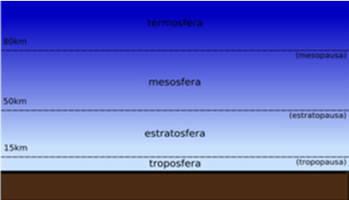
A camada de ozônio é uma região que fica na estratosfera, situada em uma altitude entre 20 a 35 km, e que é formada por ozônio(O3(g)), um gás levemente azulado de cheiro forte. Essa camada é importante porque o ozônio possui a capacidade de absorver grande parte da radiação ultravioleta (UV) do Sol, que poderia causar grandes danos aos humanos. Para saber sobre esses danos, leia o texto Consequências da destruição da camada de ozônio.

Tópicos deste artigo
- 1 - Causas da destruição da camada de ozônio
- 2 - Como os CFCs destroem a camada de ozônio?
- 3 - Consequências da destruição da camada de ozônio
Causas da destruição da camada de ozônio
Infelizmente, porém, no início da década de 1970, o radioquímico americano F. Sherwood Rowland e o químico mexicano Mário J. Molina confirmaram que essa tão preciosa camada protetora da Terra estava sendo destruída por gases produzidos pelo homem. Depois de muitas pesquisas, concluiu-se que os principais gases responsáveis pela destruição da camada de ozônio eram os CFCs (Clorofluorcarbonetos, também conhecidos como gases Fréons®), que são compostos formados por átomos de carbono, flúor e cloro.
Os CFCs são lançados na atmosfera principalmente pelo seu uso como propelente de aerossóis (sprays), seu uso em compressores para refrigeração doméstica (geladeiras, por exemplo) e para expansão de polímeros (plásticos).
Como os CFCs destroem a camada de ozônio?
Bem, vamos entender primeiro a composição química dessa camada para saber quais são as substâncias presentes nela. O gás oxigênio (O2(g)) sofre decomposição pela radiação ultravioleta do Sol e forma átomos de oxigênio livres que, por sua vez, reagem com moléculas de gás oxigênio e produzem o gás ozônio na estratosfera. Veja:
O2(g) → 2 O(g)
gás átomos de
oxigênio oxigênio livres
O(g) + O2(g) → O3(g)
átomos de gás ozônio
?oxigênio livres oxigênio
O ozônio também pode sofrer decomposição pela radiação UV e formar novamente o gás oxigênio e átomos de oxigênio livres que, conforme você verá adiante, intensificam o problema da destruição da camada de ozônio.
Quando algum gás CFC ou os halônios (substâncias de carbono e cloro que também contêm bromo) são lançados na atmosfera, suas moléculas também sofrem decomposição (são fotolizadas) pela radiação do sol e são formados átomos de cloro, fluor e carbono. Vamos considerar como exemplo o clorometano:
CH3Cl(g) → CH3(g) + Cl(g)
Esse átomo de cloro reage com as moléculas de ozônio, diminuindo a sua concentração na atmosfera e causando a destruição da camada de ozônio:
Cl(g) + O3(g) → ClO(g) + O2(g)
Fatalmente, porém, o problema não acaba por aí, o pior é que há um processo catalítico em que um único cloro provoca a destruição de centenas de milhares de moléculas de ozônio. Isso ocorre porque o ClO formado nessa última reação pode reagir com os átomos de oxigênio livres na estratosfera e formar mais átomos de cloro que destruirão as moléculas de ozônio:
ClO(g) + O(g) → Cl(g) + O2(g)
Em regiões onde a concentração de oxigênio livre é baixa, como na Antárdida, essa regeneração do cloro ocorre pela reação entre as moléculas do monóxido de cloro:
2 (Cl(g) + O3(g) → ClO(g) + O2(g))
ClO(g) + ClO(g) → Cl2O2(g)
Cl2O2(g) + luz → Cl(g) + ClOO(g)
ClOO(g)→ Cl(g) + O2(g)
Além do mais, átomos de oxigênio livres também podem reagir com moléculas de ozônio, degradando-as:
O3(g) + O(g) → O2(g) + O2(g)
É um ciclo de destruição! Um único átomo de cloro pode destruir um milhão de moléculas de ozônio!
Para agravar ainda mais a situação, os CFCs são bastante inertes, o que significa que o tempo de permanência médio deles na atmosfera é grande, variando de 75 (CFC-11) até 380 anos (CFC-115).
O bromo proveniente dos halônios e o brometo de metila também destroem o ozônio, sendo ainda mais reativos que o cloro, mas estão presentes em menor quantidade na atmosfera.
Consequências da destruição da camada de ozônio
-
Impactos sobre o organismo humano: envelhecimento precoce, mutação genética, problemas no sistema imunológico e câncer de pele.
-
Impacto sobre as plantas: comprometimento do processo de fotossíntese, impactando o sistema nutritivo das plantas e o seu crescimento.
-
Redução de espécies: Aasuperexposição de raios UV pode prejudicar o desenvolvimento de diversas espécies marítimas, como peixes, camarões, caranguejos e fitoplânctons (base da cadeia alimentar marítima). Além disso, o contato com essa radiação pode causar diversas mutações genéticas, alterando totalmente o DNA dos seres vivos.
-
Contribuição para o aquecimento global: a diminuição da camada de Ozônio e o aumento da quantidade de raios UV podem contribuir para a aceleração do aquecimento global.
Leia mais sobre o assunto: Consequências da destruição da camada de ozônio