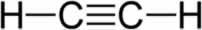Os alcinos são compostos orgânicos de cadeia aberta formados apenas por átomos de carbono e hidrogênio e possuem obrigatoriamente uma ligação tripla entre dois de seus carbonos. Podem ser classificados em verdadeiros ou falsos.
A classificação dos alcinos tem grande influência nas reações orgânicas das quais esses compostos participam.
Tópicos deste artigo
- 1 - Alcinos verdadeiros
- 2 - Alcinos falsos
- 3 - a) Em reações de hidrogenação ou halogenação
- 4 - b) Reações de adição por halogenidretos
- 5 - c) Reações de adição por hidratação
- 6 - a) Oxidação branda de um alcino verdadeiro
- 7 - b) Oxidação branda de um alcino falso
- 8 - c) Oxidação energética de um alcino falso
- 9 - d) Oxidação energética de um alcino verdadeiro
Alcinos verdadeiros
Um alcino é considerado verdadeiro quando pelo menos um dos carbonos que realizam a ligação tripla apresenta um átomo de hidrogênio:
![]()
Exemplos de cadeias de alcinos verdadeiros
Observe na imagem que, na estrutura 1, todos os carbonos da tripla apresentam um átomo de hidrogênio ligado a eles; na estrutura 2, apenas o carbono de número 1 apresenta hidrogênio. Os dois são alcinos verdadeiros.
Alcinos falsos
Um alcino é considerado falso quando nenhum dos carbonos que realizam a ligação tripla apresenta um átomo de hidrogênio:
![]()
Exemplo de cadeia de alcino falso
Observe que na estrutura acima os carbonos da tripla (de número 2 e 3) não apresentam átomo de hidrogênio.
-
Influência da classificação dos alcinos em uma reação orgânica de adição
a) Em reações de hidrogenação ou halogenação
Em reações de adição por halogenação ou hidrogenação de alcinos (verdadeiros ou falsos), ocorre o seguinte:
-
Rompimento de uma (adição parcial) ou duas (adição total) ligações pi da ligação tripla, formando uma ou duas valências livres em cada um dos carbonos envolvidos.
-
Ligação de um átomo de halogênio (Cl, Br ou I) ou hidrogênio (H) em cada uma das valências livres formadas.
Cada carbono da ligação tripla do alcino recebe o mesmo tipo de átomo em uma reação de adição como essas apresentadas.
b) Reações de adição por halogenidretos
Nessas reações, há inicialmente o rompimento de uma (adição parcial) ligação pi da tripla, o que gera duas valências livres em cada um dos carbonos envolvidos.
Assim, um carbono recebe um hidrogênio, e o outro recebe o halogênio. Logo em seguida, a outra ligação pi é rompida, formando duas novas valências. O halogênio liga-se ao carbono menos hidrogenado, e o hidrogênio, ao mais hidrogenado (segundo a regra de Markovnikov).
Obs.: Caso esse tipo de reação ocorra em um alcino falso, o halogênio será adicionado ao carbono da tripla mais próximo da extremidade da cadeia, em razão do efeito indutivo.
c) Reações de adição por hidratação
A reação de hidratação de um alcino (falso ou verdadeiro) ocorre sempre de forma monomolecular, ou seja, apenas uma molécula de água é adicionada ao alcino, a partir do rompimento de uma ligação pi da tripla.

Equação da hidratação de um alcino verdadeiro
De acordo com a regra de Markovnikov, o carbono mais hidrogenado recebe o hidrogênio, e o menos hidrogenado recebe a hidroxila. O resultado é a formação de um enol (composto orgânico extremamente instável), que automaticamente sofre uma interconversão:

Interconversão do enol formado na adição do alcino verdadeiro
A ligação pi da dupla estabelece-se entre o carbono e o oxigênio. O hidrogênio que estava com o oxigênio é transferido para o outro carbono da dupla.
-
Influência da classificação dos alcinos em uma reação orgânica de oxidação
As reações orgânicas de oxidação podem ocorrer de forma branda (em presença de água, base e permanganato de potássio) ou energética (em presença de água, ácido e permanganato de potássio). Veja as características dessas reações em cada tipo de alcino:
a) Oxidação branda de um alcino verdadeiro
Inicialmente ocorre o rompimento das duas ligações pi da tripla, formando quatro valências livres, duas em cada um dos carbonos. Essas valências livres são preenchidas por grupos hidróxidos (OH).
.jpg)
Representação do rompimento de duas ligações pi
Como a presença de duas hidroxilas em um carbono torna-o instável, temos uma consequente desidratação, ou seja, em cada átomo de carbono ocorre a formação de uma molécula de água. Já entre o oxigênio restante e o carbono, ocorre a formação de uma ligação dupla.

Equação da desidratação em alcino verdadeiro
Quando um alcino verdadeiro participa de uma oxidação branda, ocorre a formação de um aldeído gêmino.
b) Oxidação branda de um alcino falso
Acontece da mesma forma que o processo ocorrido no alcino verdadeiro. A diferença entre os dois é que, se o carbono da tripla apresentar hidrogênio (alcino verdadeiro), formará aldeído; se não apresentar hidrogênio (alcino falso), formará uma cetona.
.jpg)
Equação representando a desidratação de alcino falso
Um alcino falso, ao participar de uma oxidação branda, gera uma cetona gêmina.
c) Oxidação energética de um alcino falso
Inicialmente ocorre o rompimento de todas as ligações presentes na tripla, formando seis valências livres, três em cada um dos carbonos. Essas valências livres são preenchidas por grupos hidróxidos (OH).

Representação do rompimento de toda a ligação tripla
Como a presença de três hidroxilas em um carbono torna-o instável, temos uma consequente desidratação, ou seja, em cada átomo de carbono ocorre a formação de uma molécula de água. Já entre o oxigênio restante e o carbono, ocorre a formação de uma ligação dupla.

Equação da desidratação em alcino falso
Um alcino falso, ao participar de uma oxidação energética, gera dois ácidos carboxílicos (iguais ou diferentes).
d) Oxidação energética de um alcino verdadeiro
Inicialmente ocorre o rompimento de todas as ligações presentes na tripla, formando seis valências livres, três em cada um dos carbonos. Essas valências livres são preenchidas por grupos hidróxidos (OH). O hidrogênio que estava ligado ao carbono da tripla também é oxigenado, formando mais um grupo OH.
Como a presença de três hidroxilas em um carbono torna-o instável, temos uma consequente desidratação, ou seja, em cada átomo de carbono ocorre a formação de uma molécula de água. Já entre o oxigênio restante e o carbono, ocorre a formação de uma ligação dupla.

Equação representando a desidratação de alcino verdadeiro
Como resultado, um alcino verdadeiro, ao participar de uma oxidação energética, forma ácido carboxílico com gás carbônico ou apenas moléculas de gás carbônico.
Videoaula relacionada: