A Cinética Química estuda a velocidade com que as reações ocorrem. A partir desse estudo é possível retardar ou aumentar a rapidez de várias reações.
Isso é extremamente importante em nosso dia a dia e, principalmente, nas indústrias químicas, que perderiam muito dinheiro se determinadas reações continuassem ocorrendo de forma muito lenta.
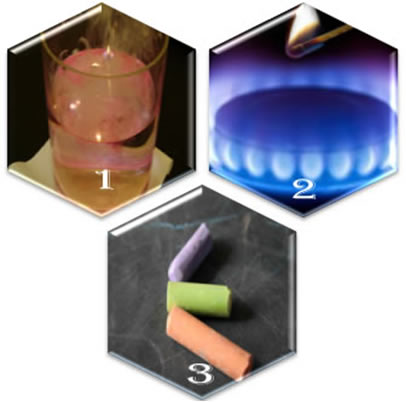
Um exemplo é o mostrado na figura, onde a mistura de líquidos para foguetes (em que o hidrogênio é o combustível, e o oxigênio é o comburente) só ocorre de maneira rápida em virtude da ação de uma faísca elétrica ou de uma chama; do contrário, a reação ocorreria de forma tão lenta que seria impossível determinar sua velocidade.
Esse ramo da Química mostra como é possível calcular a taxa de variação da rapidez de uma reação, quais são os fatores que influenciam na velocidade das reações e quais são as condições necessárias para que uma reação ocorra. Além disso, explica vários conceitos, como: energia de ativação, complexo ativado, teoria das colisões, catalisadores, ordem de uma reação, etc.
Entenda essas e outras questões nesta subseção.