Cálculos da tonoscopia são operações matemáticas realizadas com o objetivo de determinar o quanto a pressão máxima de vapor de um solvente diminui ao ser adicionado a ele um soluto não volátil.
Se, por exemplo, temos 500 L de água em um reservatório fechado, seu vapor exerce uma pressão máxima de vapor p2 nas paredes do recipiente. Porém, se adicionarmos 100 g de cloreto de sódio a essa água, haverá uma menor evaporação do líquido e, consequentemente, uma nova pressão de vapor p.
.jpg)
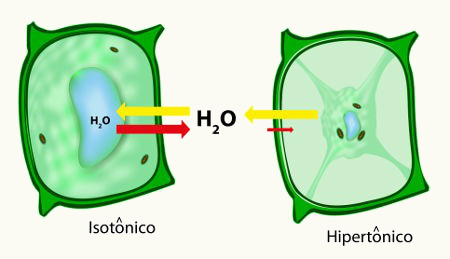
Quanto mais soluto um solvente tiver, menor será sua pressão de vapor
A partir dos cálculos da tonoscopia, podemos determinar os valores dessas pressões de forma individual e ainda:
-
A variação da pressão máxima de vapor;
-
A massa de soluto necessária para modificar a pressão;
-
A massa molar do soluto utilizado para modificar a pressão;
-
A constante do líquido utilizado;
-
A massa do solvente presente no recipiente.
Fórmulas utilizadas em cálculos da tonoscopia
→ Abaixamento absoluto (Δp)
Δp = p-p2
-
p = pressão máxima de vapor do solvente na solução;
-
p2 = pressão máxima de vapor do solvente.
→ Abaixamento relativo envolvendo fração molar
Δp = X1
p2
-
X1 = fração molar do soluto.
→ Abaixamento relativo envolvendo molalidade
Δp = Kt.W
p2
-
Kt = constante tonoscópica;
-
W = molalidade (concentração em mol/Kg).
Como a molalidade é a relação da massa do soluto (m1) pelo produto da massa molar do soluto (M1) com a massa do solvente (m2), podemos reescrever a fórmula do abaixamento relativo da seguinte maneira:
Δp = Kt.m1
p2 M1.m2
Obs.: Caso a solução apresente um soluto iônico (que dissocia ou ioniza), é fundamental que seja determinado o fator de Van't Hoff (que corrige o número de partículas presentes na solução) pela seguinte expressão:
i = 1 + α.(q-1)
-
i = fator de Van't Hoff
-
α = grau de ionização ou dissociação
-
q = número de partículas
Exemplos de aplicação dos cálculos da tonoscopia
1º Exemplo: Sabendo que a pressão de vapor de uma solução não eletrolítica, contendo 80 g de um soluto qualquer em 360 g de água, é 315 mmHg a 80 °C, calcule a massa molar do soluto do soluto utilizado no preparo da solução. Dado: pressão máxima de vapor da água a 80 °C é 355 mmHg e kt = 1,8 . 10-2.
O enunciado fornece os seguintes dados:
-
Massa do soluto (m1) = 80 g
-
Massa do solvente (m2) = 360 g ou 0,36 Kg (após dividir por 1000, pois a unidade da massa do solvente deve ser trabalhada em quilogramas)
-
Pressão máxima de vapor do solvente (p2) = 315 mmHg
-
Pressão máxima de vapor do solvente na solução (p) = 355 mmHg
-
Kt = 1,8.10-2 ou 0,018
-
Massa molar do soluto (M1) = ?
Para determinar a massa molar do soluto, de acordo com os dados fornecidos, devemos utilizar a fórmula do abaixamento relativo que contém os elementos da molalidade (M1, m1 e m2), como a seguir:
Δp = Kt.m1
p2 M1.m2
p-p2 = Kt.m1
p2 M1.m2
355-315 = 0,018.80
355 M1.0,36
40 = 1,44
355 M1.0,36
40.M1.0,36 = 355.1,44
14,4.M1 = 511,2
M1 = 511,2
14,4
M1 = 35,5 g/mol
2º Exemplo: Em um recipiente contendo 0,8 L de água a 90 °C, foram adicionados 180 g de NaCl, os quais foram totalmente solubilizados. Admitindo que esse sal esteja totalmente dissociado em meio aquoso (grau de dissociação de 100%), qual é o valor do abaixamento relativo da pressão máxima de vapor promovido? Dados: kt = 0,018.
Dados fornecidos pelo exercício:
-
Grau de ionização = 100% ou 1 (após ser dividido por 100)
-
Massa do soluto = 190 g
-
Volume do solvente (V2) = 0,8 L ou 800 mL (após multiplicar por 1000)
-
kt = 0,018
-
Abaixamento relativo da pressão de vapor = ?
Não pare agora... Tem mais depois da publicidade ;)
1º Passo: Determinar o fator de Van't Hoff.
Para isso, devemos utilizar o grau de ionização (1) e o número de partículas (2, pois temos 1 cátion de Na+ e 1 ânion de Cl-1) na expressão a seguir:
i = 1 + α.(q-1)
i = 1 + 0,13.(2-1)
i = 1 + 0,13.1
i = 1 + 0,13
i = 1,13
2º Passo: Calcular a massa molar do soluto.
Para isso, devemos multiplicar a quantidade de átomos de cada elemento pela sua massa atômica e, em seguida, somar os resultados:
M1 = 1.23 + 1.35,5
M1 = 23 + 35,5
M1 = 58,5 g/mol
3º Passo: Calcular a massa da água.
O exercício indicou o volume da água, 0,8 L, e como a densidade da água é de 1 Kg/L, temos que:
d2 = m2
V2
1 = m2
0,8
m2 = 1.0,8
m2 = 0,8 Kg
4º Passo: Utilizar os dados fornecidos e a massa calculada no passo anterior na expressão do abaixamento relativo contendo os elementos da molalidade (M1, m1 e m2), como a seguir:
Δp = Kt.m1 .i
p2 M1.m2
Δp = 0,018.190 .2
p2 58,5.0,8
Δp = 6,84
p2 46,8
Δp = 0,146
p2
3º Exemplo: Uma solução aquosa, de concentração em massa 16% de ácido fosfórico, H3PO4(aq), encontra-se 13% ionizada. Qual será valor do abaixamento relativo da pressão máxima de vapor nessa solução?
Dados fornecidos pelo exercício:
-
Grau de ionização = 13% ou 0,13 (após ser dividido por 100)
-
Porcentagem em massa = 16%
-
Fração molar do soluto (X1) = 0,16 (que é o resultado da porcentagem em massa após ser dividida por 100)
-
Abaixamento relativo da pressão de vapor = ?
De acordo com os dados fornecidos pelo exercício, para determinar o valor do abaixamento relativo da pressão, são necessários os seguintes passos:
1º Passo: Determinar o fator de Van't Hoff.
Para isso, devemos utilizar o grau de ionização (0,03) e o número de partículas (3) na expressão a seguir:
i = 1 + α.(q-1)
i = 1 + 0,13.(2-1)
i = 1 + 0,13.1
i = 1 + 0,13
i = 1,13
2º Passo: Utilizar os dados fornecidos pelo exercício e fator de Van't Hoff encontrado no primeiro passo na expressão do abaixamento relativo contendo a fração molar do soluto e o fator:
Δp = X1.i
p2
Δp = 0,16.1,13
p2
Δp = 0,18
p2
4º Exemplo: Determine a massa de sacarose (C12H22O11), que foi dissolvida em 1200 g de água, suficiente para causar um abaixamento relativo da pressão máxima de vapor igual a 0,008.
Os dados fornecidos pelo exercício foram:
-
Abaixamento relativo da pressão máxima de vapor = 0,008
-
Massa de água (m2) = 1200 g ou 1,2 Kg (após dividir por 1000, pois a unidade da massa do solvente deve ser trabalhada em quilogramas)
-
Massa do soluto (m1) = ?
Para determinar a massa do soluto, é necessária a realização dos seguintes passos:
1º Passo: Calcular a massa molar do soluto.
Para isso, devemos multiplicar a quantidade de átomos de cada elemento pela sua massa atômica e, em seguida, somar os resultados:
M1 = 12.12 + 22.1 + 11.16
M1 = 144 + 22 +176
M1 = 342 g/mol
2º Passo: Calcular a massa molar da água.
M2 = 2.1 + 1.16
M2 = 2 + 16
M2 = 18 g/mol
3º Passo: Determinar o kt da água.
Para isso, basta dividir a massa molar da água encontrada no segundo passo por 1000:
kt = M2
1000
Kt = 18
1000
kt = 0,018
4º Passo: Utilizar os dados fornecidos e a massa calculada no primeiro passo na expressão do abaixamento relativo contendo os elementos da molalidade (M1, m1 e m2), como a seguir:
Δp = Kt.m1
p2 M1.m2
0,008 = 0,018.m1
342.1,2
0,008.342.1,2 = 0,018.m1
3,2832 = 0,018.m1
3,2832 = m1
0,018
m1 = 182,4 g