As propriedades coligativas estudam o efeito dos solutos não voláteis em uma solução, fato esse que não é diferente na osmoscopia (propriedade que estuda a relação entre pressão osmótica e osmose).
Os cálculos na osmoscopia envolvem vários aspectos importantes, sendo o mais relevante deles a pressão osmótica. Denomina-se de pressão osmótica a força exercida pela solução menos concentrada sobre a membrana semipermeável, ou seja, é a força contrária à ocorrência da osmose. Veja um exemplo:
.jpg)
Ocorrência da osmose entre soluções salinas
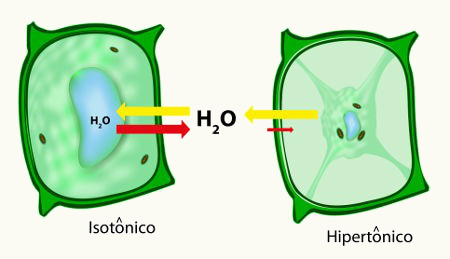
A solução 1 é menos concentrada que a solução 2, ou seja, na solução 1, temos uma maior quantidade de água em relação à quantidade de sal (NaCl). Por essa razão, parte da água da solução 1 atravessa a membrana semipermeável em direção à solução 2. Esse fenômeno é o que chamamos de osmose.
Durante a ocorrência da osmose, a solução 2 começa a exercer uma força (pressão osmótica) sobre a membrana semipermeável para tentar evitar a passagem do solvente. A pressão osmótica é representada pela letra grega pi (π).
Fórmula para cálculo com soluto molecular
A fórmula mais utilizada em cálculos na osmoscopia é:
π = M.R.T
-
π = pressão osmótica;
-
M = concentração em mol/L;
-
R = constante geral dos gases (0,082 para atm e 62,3 para mmHg);
-
T = temperatura em Kelvin.
Dica: Para converter uma temperatura em graus Celsius para Kelvin, basta somar o valor com 273.
Essa fórmula é utilizada apenas quando o soluto presente na solução estudada é molecular, ou seja, o soluto não sofre ionização nem dissociação.
Fórmula para cálculo com soluto iônico
Quando a solução é formada por um soluto não volátil de natureza iônica, ou seja, que sofre o fenômeno da ionização ou dissociação, devemos utilizar a fórmula descrita acima da seguinte forma:
π = M.R.T.i
O i é o fator de correção de Van't Hoff, o qual deve ser calculado pela seguinte equação:
i = 1 + α.(q-1)
-
i = fator de correção de Van't Hoff;
-
α = grau de ionização ou dissociação do soluto;
-
q = número de íons liberados ou produzidos pelo soluto em solução.
Interpretações realizadas a partir dos cálculos na osmoscopia
-
Solução isotônica
É a solução que apresenta a mesma pressão osmótica que a outra solução.
π1 = π2
-
Solução hipertônica
É a solução (solução 1) cuja pressão osmótica é maior que a da outra solução (solução 2):
π1 > π2
-
Solução hipotônica
É a solução (solução 1) cuja pressão osmótica é menor que a da outra solução (solução 2):
π1 < π2
Exemplos
1º) (PUC-RS) Eventualmente, a solução 0,30 M de glicose é utilizada em injeção intravenosa, pois tem pressão osmótica próxima à do sangue. Qual a pressão osmótica, em atmosferas, da referida solução a 37 °C?
a) 1,00
b) 1,50
c) 1,76
d) 7,63
e) 9,83
Dados fornecidos pelo exercício:
-
Concentração em mol/L = 0,30 M
-
π = ?
-
Temperatura = 37oC, mas, em Kelvin, é igual a 310 K
-
R = 0,082 (padrão utilizado quando o exercício não menciona unidade de pressão)
Para determinar a pressão osmótica, basta utilizar os valores fornecidos na expressão a seguir:
π = M.R.T
π = 0,3.0,082.310
π = 7,626 atm
ou
π = 7,63 atm aproximadamente.
2º) (Hermânio Ometto-SP) O sangue humano tem pressão osmótica 7,8 atm. a 37º C. A massa aproximada de cloreto de sódio que deve ser dissolvida em água, suficiente para preparar 4 litros de solução isotônica, a ser usada nessa temperatura é:
a) 9 g
b) 18 g
c) 27 g
d) 36 g
e) 45 g
Dados fornecidos pelo exercício:
-
Volume da solução = 4 L
-
π = 7,8 atm
-
Temperatura = 37oC, mas, em Kelvin, é igual a 310 K
-
R = 0,082 (padrão utilizado quando o exercício não menciona unidade de pressão)
-
Massa do soluto na solução = ?
Não pare agora... Tem mais depois da publicidade ;)
Como a solução preparada é isotônica em relação ao sangue, consideramos a pressão osmótica da solução igual a 7,8 atm. Assim, para determinar a massa de cloreto de sódio, devemos fazer o seguinte:
Passo 1: determinar a massa molar do cloreto de sódio.
Para isso, basta multiplicar a massa de cada elemento pela sua quantidade de átomos na fórmula química e depois somar os resultados:
M1 = 1.23 + 1.35,5
M1 = 23 + 35,5
M1 = 58,5 g/mol
Passo 2: determinar o fator de correção de Van't Hoff do NaCl, já que ele é um soluto iônico.
Para tal, vamos levar em consideração que o grau de dissociação do sal é de 100%, já que não foi informado, e que o seu número de íons liberados (q) é igual a 2, já que temos apenas um átomo de Na e um de Cl.
i = 1 + (q-1)
i = 1 + 1.(2-1)
i = 1 + 1. (1)
i = 1 + 1
i = 2
Passo 3: determinar a massa do soluto.
Para determinar a massa, basta utilizar os valores fornecidos na expressão a seguir, na qual substituímos a concentração molar pela massa do soluto dividida pelo produto da massa molar e do volume:
π = m1 .R.T.i
M1.V
7,8 = m1 . 0,082.310.2
58,5.4
58,5.4.7,8 = 50,84m1
50,84m1 = 1825,2
m1 = 1825,2
50,84
m1 = 35,9 g (aproximadamente)
3º) (UFMS) Em meio aquoso, uma solução 0,13 mol.L-1 de glicose a – 23ºC é isotônica de uma solução de cloreto de cálcio a 27ºC. Sabendo-se que o fator de Van’t Hoff (i) é igual a [1+?(q-1)] e que o grau de dissociação iônica do sal é de 80%, calcule a concentração em quantidade de matéria da solução de cloreto de cálcio. Para efeito de resposta, expresse o resultado em mmol.L-1, com dois algarismos significativos.
O exercício apresenta dados de duas soluções: glicose e cloreto de cálcio.
-
Concentração em mol/L da solução de glicose = 0,13 mol.L-1
-
π da solução de glicose = ?
-
Temperatura da solução de glicose = -23 oC (em Kelvin, é igual a 250 K)
-
R = 0,082
-
Temperatura da solução de cloreto de cálcio = 27oC (em Kelvin, é igual a 300 K)
-
π da solução de cloreto de cálcio = ?
-
grau de ionização ou dissociação do cloreto de cálcio = 80%
Para determinar a concentração em quantidade de matéria do cloreto de cálcio, devemos fazer o seguinte:
Passo 1: determinar a pressão osmótica da solução de glicose.
π = M.R.T
π = 0,13.0,082.250
π = 2,665 atm
A pressão osmótica da solução de glicose foi calculada porque ela é isotônica da solução de cloreto de cálcio. Assim sendo, a pressão osmótica do cloreto de cálcio é igual a 2,665 atm.
Passo 2: cálculo da massa molar do cloreto de cálcio.
Para isso, basta multiplicar a massa de cada elemento pela sua quantidade de átomos na fórmula química e depois somar os resultados:
M1 = 1.40 + 2.35,5
M1 = 40 + 71
M1 = 111 g/mol
Passo 3: determinar o fator de correção de Van't Hoff do CaCl2, já que ele é um soluto iônico.
Para tal, vamos utilizar o grau de dissociação do sal fornecido (80%) e o número de íons liberados (q), que é 3, já que temos apenas um átomo de Ca e dois de Cl, os quais são liberados durante a dissociação:
i = 1 + (q-1)
i = 1 + 0,8.(3-1)
i = 1 + 0,8. (2)
i = 1 + 1,6
i = 2,6
Passo 4: calcular a concentração em quantidade de matéria (mol/L) da solução de cloreto de cálcio.
π = M.R.T.i
2,665 = M.0,082.300.2,6
2,665 = M.63,96
M = 2,665
63,96
M = 0,041666mol/L
ou
M = 0,042 mol/L (aproximadamente)
Passo 5: converter o resultado para mmol/L.
Para isso, basta multiplicar o resultado por 100:
M = 0,042 mol/L.1000
M = 42 mmol/L