“A Terra é azul!” – essa foi a exclamação feita no dia 12 de abril de 1961, pelo cosmonauta soviético Yury Gagarin ao realizar o primeiro voo ao redor da órbita da Terra.
Hoje praticamente todas as pessoas sabem que a quantidade aproximada de água cobrindo a superfície terrestre é de 70%, ou seja, 1,4 bilhão de km3 do volume da Terra é constituído de água.
No entanto, mesmo conhecendo bem esse fato, não percebemos no cotidiano a importância da água para a nossa vida. Além disso, muitos não conhecem as propriedades interessantes que só a água tem e que fazem com que esse líquido seja tão precioso.
Mas antes de vermos o que torna a água uma substância tão interessante, vamos primeiramente conceituar a que estamos nos referindo. Por que isso é necessário? Basicamente por dois motivos: o primeiro está relacionado ao fato de haver diferentes significados para ela na Química. Por exemplo, a água pode ser um material que contém diversas substâncias dissolvidas (como a água da torneira, a água da chuva, a água mineral, a água subterrânea, a água do mar, etc.) ou então somente a substância pura com a fórmula molecular H2O, isto é, suas moléculas são formadas por dois átomos de hidrogênio ligados a um átomo de oxigênio (que é o caso da água destilada ou desmineralizada). O segundo motivo é que só sabendo dessa constituição da água é que poderemos entender suas características peculiares.
Uma dessas características é o fato de que só a água é encontrada na natureza nos três estados físicos: nos rios, lagos e mares ela está na forma líquida; na atmosfera, encontra-se na forma de vapor; e nas calotas polares, está na forma sólida (gelo).
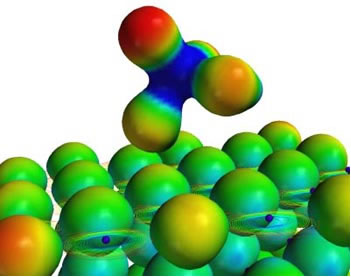
Uma série de propriedades características da água resulta simplesmente da sua geometria molecular, na qual o ângulo formado é de 104º40’, conforme a figura a seguir. A forma angular da molécula de água é assim, porque, visto que o oxigênio possui dois pares eletrônicos que não participam das ligações com os hidrogênios, eles repelem os outros dois pares eletrônicos que participam das ligações químicas. Isso faz com que ocorra uma retração no ângulo da molécula.

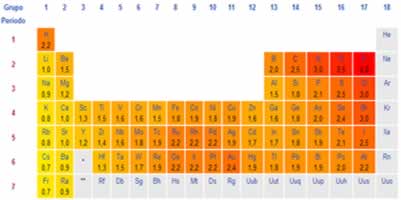
Essa forma angular é a responsável pela formação de ligações de hidrogênio entre uma molécula de água com as outras que estão ao seu redor. Além disso, outro fator que ocasiona as ligações de hidrogênio é que a molécula de água é polar, isto é, há uma diferença de eletronegatividade entre o oxigênio – que constitui o polo negativo – e os hidrogênios – polos positivos. Pelo fato de o ângulo ser de 104º40’ na molécula de água, os dipolos da molécula não se anulam, conferindo polaridade a ela e havendo, portanto, atração entre uma molécula e as outras.

Essas ligações são responsáveis pela tensão superficial da água, que faz com que os insetos possam se locomover em cima dela. Também são responsáveis pelas elevadas temperaturas da água em relação a outras substâncias de mesma massa molecular e também fazem com que o gelo seja menos denso que a água, flutuando nela.

Essa última característica da água é realmente muito interessante, pois se compararmos com outros materiais, veremos que ao ficarem sólidos sua densidade fica maior. Já com a água não é assim: quando as moléculas de água têm a sua temperatura diminuída elas se aproximam mais, e isso faz com que as ligações de hidrogênio se organizem num arranjo hexagonal, com uma estrutura cristalina em que há espaços vazios em seu interior. O resultado é que o gelo é menos denso que a água e flutua sobre ela.

Graças a essa propriedade incomum da água é que ocorre a manutenção da vida. Pois é por isso que o gelo formado nos lagos e mares ficam na superfície desses. Quando a temperatura se eleva, eles derretem; mas, se fosse o contrário, se o gelo fosse mais denso e afundasse, dificilmente ele derreteria. Além disso, a água atinge sua densidade máxima a 4ºC, ainda no estado líquido. Assim, quando as águas superficiais atingem essa temperatura, elas tornam-se mais densas e afundam, causando o fenômeno de convecção, que mistura os nutrientes dissolvidos à água, que mantém a vida de inúmeras espécies animais e vegetais.
Outro fator interessante da água que é causado também pelas ligações de hidrogênio é o elevado calor específico dela (4, 184 J/gºC ou aproximadamente 4,2 joules). A vida na Terra é extremamente favorecida por essa propriedade da água, pois permite que ela absorva grandes quantidades de energia com pequenas variações de temperatura. Isso faz com que a Terra não sofra variações tão bruscas de temperatura entre o dia e a noite, pois a água da atmosfera e da superfície absorve grande quantidade de calor durante o dia, e durante a noite devolve esse calor para o ambiente.
Pelo processo das correntes marítimas e pela evaporação e condensação da grande quantidade de água na superfície terrestre, o fluxo da energia térmica absorvida pela radiação solar é facilitado.
A água possui diversos aspectos exclusivos dela, mas um último aspecto interessante e importante da água que iremos citar é que ela é capaz de dissolver grandes quantidades de substâncias e materiais, sendo, portanto, denominada solvente universal. Essa facilidade de dissolver diferentes tipos de substâncias também se deve à geometria e à disposição de suas cargas. A polarização da água permite que ela separe íons de outras substâncias, o que permite a ocorrência de diversos processos químicos, físicos e biológicos.