Inicialmente, tanto no conceito dos filósofos gregos, quanto no conceito de Dalton, achava-se que o átomo era uma partícula indivisível. No entanto, com o passar do tempo e com o avanço dos métodos científicos, por meio de experimentos abalizados, foi possível descobrir que na verdade o átomo é divisível.
Ele é composto por três partículas subatômicas principais, que são: elétrons, prótons e nêutrons. Observe na tabela abaixo algumas características de cada uma dessas partículas e, em seguida, como foram descobertas.


• Elétrons (e-): essa foi a primeira partícula a ser descoberta. Desde a Antiguidade, cerca de 2500 anos atrás, na Grécia antiga, já se conhecia a natureza elétrica da matéria. Porém, somente em 1856 é que foi comprovada a existência do elétron no átomo. Os cientistas Geissler e Crookes usaram um tubo de raios catódicos em que, ao se aplicar uma ddp (diferença de potencial) muito alta, era possível ver um feixe de luz (raios catódicos) que ia na direção do polo positivo.
Visto que cargas opostas se atraem, em 1897, J. J. Thomson (1856-1940) provou que esse feixe ordenado era composto de partículas subatômicas que tinham uma carga elétrica negativa e recebeu o nome de elétron (termo que tem origem no grego élektron, que significa âmbar – resina que era atritada e atraía pequenos objetos). Ele fez isso por determinar que a relação da carga do elétron e de sua massa apresentava o mesmo valor (e/m = 1,758805 . 1011 C. kg-1), independente do gás que estivesse no tubo ou na ampola. Se não importava qual gás era usado no experimento, isso significava que o elétron fazia parte do componente básico de qualquer matéria, o átomo.
Segundo o modelo atômico de Rutherford-Böhr, essa partícula permanece girando ao redor do núcleo, em uma região denominada eletrosfera, e sua energia varia de átomo para átomo, pois depende da camada eletrônica em que ele se apresenta, no seu estado fundamental.

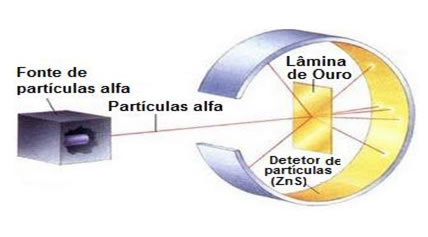
• Prótons (p): segunda partícula a ser descoberta. Esse fato ocorreu em 1904, pelo cientista Ernest Rutherford (1871-1937) e sua equipe de trabalho. Eles usaram um tubo parecido com o tubo de raios catódicos, porém o gás que o preenchia era o gás hidrogênio e observaram um feixe que ia no sentido do polo negativo. Assim, foi comprovada a existência na estrutura do átomo de partículas positivas, que foram denominadas prótons (p), que vem do grego prôtos, que significa “primeiro”.
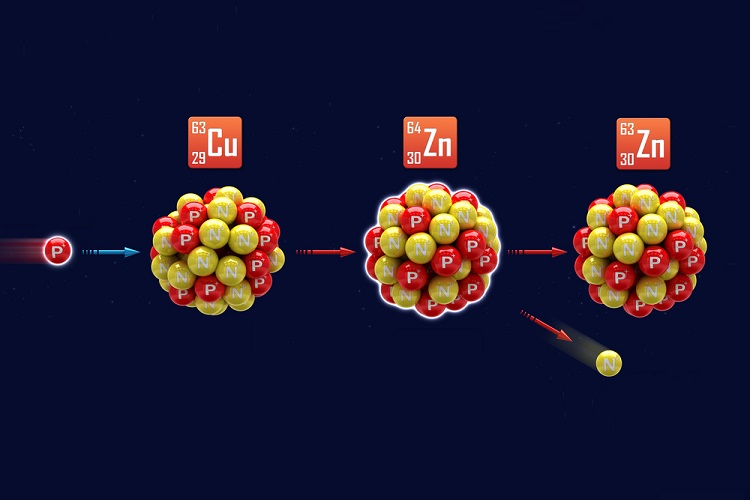
Essa partícula permanece no núcleo do átomo e só sofre mudança em reações nucleares de fusão ou fissão. Ela tem intensidade de carga elétrica igual a do elétron, porém com sinal oposto.
• Nêutrons (n): o modelo atômico até então dizia que o átomo tinha um núcleo positivo, com prótons e uma eletrosfera com partículas negativas, os elétrons. Porém, visto que cargas opostas se atraem, isso comprometia a estabilidade do átomo; os elétrons iriam perder energia e percorrer um espiral em direção ao núcleo, emitindo energia em forma de luz. Dessa forma, Rutherford admitiu que no núcleo existiam também partículas subatômicas, denominadas nêutrons, que não possuíam carga nenhuma.
Isso foi comprovado em 1932, por Chadwick, que realizou experimentos com material radioativo e descobriu essa partícula neutra, nomeando-a nêutron.
* 1 u equivale a 1,660566 . 10-27 kg.
# 1 uec equivale à unidade elementar de carga elétrica, que é 1,6 . 10-19 C.
Aproveite para conferir nossas videoaulas relacionadas ao assunto: