Geralmente, quando uma substância passa do estado líquido para o estado sólido, as substâncias se contraem, ou seja, o estado de agitação das moléculas diminui. Pelo fato de as substâncias se contraírem, a densidade tende a aumentar.
A água apresenta um comportamento diferente das demais substâncias, pois quando passa para o estado sólido, transformando-se em gelo, ela sofre uma expansão. Em consequência dessa expansão, o seu volume aumenta e a densidade diminui.
O gelo tem densidade de 0,917g/cm3 à temperatura de 0º C, por isso não afunda. Pelo fato de a água se expandir quando passa do estado líquido para o estado sólido não é recomendável que se guarde garrafa de vidro cheia de água nos congeladores.
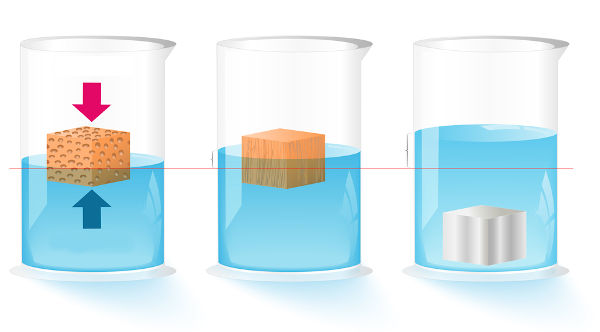
Vamos considerar a figura abaixo (um copo com água e uma pedra de gelo) e fazer uma estimativa do volume total, o quanto de gelo fica acima do nível da água. Sendo V o volume do gelo, V1 o volume emerso, VL o volume submerso, dG a densidade do gelo e dL a densidade da água.

Pelo princípio de Arquimedes temos:
Empuxo = Peso

De acordo com os cálculos, percebemos que a parte submersa é 91,7%, e a parte emersa, fora da água, é 8,3%.